品名:Customized Buffer(品番:EL005-01)
使用条件に合わせた緩衝液を作製します
緩衝液の pH は、濃度、温度、イオン強度などにより変動します。
弱酸を用いた緩衝液は希釈すると pH が上がり、弱塩基を用いた緩衝液では希釈によって逆に pH が下がります。
また、温度変化は緩衝液の解離基の pKa を変化させるため、例えばトリス緩衝液では 10 ℃ の温度変化によっておよそ 0.3 の pH 変動が見られます。
さらに、緩衝液に塩を加えるとイオン強度が高まり、活量係数が低下することによって pH が変化します。例えば、一般的なリン酸カリウム緩衝液に 50 mM の KCl を加えると pH が 0.3 以上変化します。
弊社では、 pH、濃度、温度、酸やアルカリの種類、塩類の添加の有無など、最終的なご使用条件に合わせて、ご希望の緩衝液を作製します。
活性測定やタンパク質の結晶化などにも、ぜひご活用ください。
【ご依頼いただいた例】
・20 倍希釈したときに pH 7.5 (25℃) になる 1 M HEPES Buffer
・20 倍希釈したときに pH 6.5 (25℃) になる 1 M MES Buffer
・20 倍希釈したときに pH 6.7 (25℃) になる 1 M PIPES Buffer
Good’s Buffer(グッドバッファー)
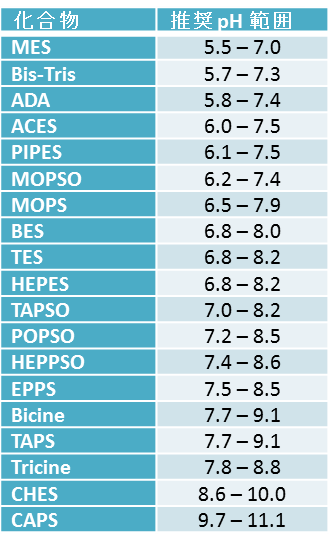
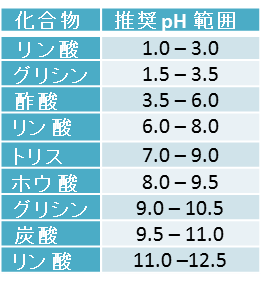
その他の緩衝液
文献例:Ferguson, W. J.et al.(1980) Anal. Chem.104, 300-310 活性測定法 − 分光学的方法 − 倉光成紀 (1991)
新生化学実験講座 第1巻 V.酵素・その他の機能タンパク質
(崎山文夫,鈴木紘一,太田隆久 編) p.37-47,東京化学同人,東京
蛋白質・酵素の基礎実験法 (堀尾武一 編) p.552-559, 南江堂, 東京
弊社学術顧問 大阪大学 名誉教授 倉光成紀 先生がご相談に応じてくださいます。
まずは弊社お問い合わせページよりお気軽にご相談ください。
【価格例】
・1 M HEPES 100 ml ¥12,000 (税抜)
・1 M HEPES-NaOH (pH 7.0) 100 ml ¥12,000 (税抜)
